| Issue |
J. Phys. II France
Volume 1, Number 10, October 1991
|
|
|---|---|---|
| Page(s) | 1179 - 1196 | |
| DOI | https://doi.org/10.1051/jp2:1991127 | |
J. Phys. II France 1 (1991) 1179-1196
Influence of electronegativity on the electronic structures and stabilities
of microclusters of carbides
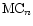 (M : transition, rare-earth or
normal element,
n < 10)
(M : transition, rare-earth or
normal element,
n < 10)
M. Leleyter Groupe de Physique Théorique, Faculté des Sciences d'Amiens, 33 rue Saint-Leu, 80039 Amiens Cedex, France also Laboratoire d'Informatique Appliquée aux Sciences Physiques, CURI, 5 rue du Moulin Neuf, 80000 Amiens, France
(Received 12 November 1990, accepted in final form 4 July 1991)
Abstract
![]() , clusters
(n < 10) produced from carbides by various experimental techniques (SIMS, SSMS, LAMMA, Knudsen effusion, etc.) show strong alternations
in their emission intensities
, clusters
(n < 10) produced from carbides by various experimental techniques (SIMS, SSMS, LAMMA, Knudsen effusion, etc.) show strong alternations
in their emission intensities
![]() according to the parity of the carbon atom number
n. Maxima take place for odd
n ("odd" alternations) if M = H, F, Cl or Fe, Ni, Rh, Ir, Pt or for even
n ("even" alternations) if M = B, Si, Ba, Ge or Sc, Ti, V, Cr, Y, Zr, La, Ce, W, Th, U or even the ions exist only for even
n (Nd, Dy, Ho, Er). Moreover, only CO,
according to the parity of the carbon atom number
n. Maxima take place for odd
n ("odd" alternations) if M = H, F, Cl or Fe, Ni, Rh, Ir, Pt or for even
n ("even" alternations) if M = B, Si, Ba, Ge or Sc, Ti, V, Cr, Y, Zr, La, Ce, W, Th, U or even the ions exist only for even
n (Nd, Dy, Ho, Er). Moreover, only CO,
![]() O, CN and
O, CN and
![]() N are known for O and N. Such phenomena are due to the stability properties of the clusters themselves ("correspondence rule")
and can be interpreted with the Pitzer and Clementi model (sp hybridization in Hückel approximation): the clusters are assumed
to be linear chains of "cumulene" type :C=C=..C=C=M and the alternations in the relative stabilities of these chains are mainly
due to the fact that the HOMO (highest occupied molecular orbital) of the clusters lies in a double degenerate
N are known for O and N. Such phenomena are due to the stability properties of the clusters themselves ("correspondence rule")
and can be interpreted with the Pitzer and Clementi model (sp hybridization in Hückel approximation): the clusters are assumed
to be linear chains of "cumulene" type :C=C=..C=C=M and the alternations in the relative stabilities of these chains are mainly
due to the fact that the HOMO (highest occupied molecular orbital) of the clusters lies in a double degenerate
![]() level band. Now HOMO may be either full or half-filled, and an aggregate with a complete (or almost complete) HOMO is more
stable than an aggregate with a half-filled HOMO. Consequently, the number of
level band. Now HOMO may be either full or half-filled, and an aggregate with a complete (or almost complete) HOMO is more
stable than an aggregate with a half-filled HOMO. Consequently, the number of
![]() electrons is governing the parity effect in the stability alternations. However, this number is depending on the number of
electrons is governing the parity effect in the stability alternations. However, this number is depending on the number of
![]() electrons of the chain and besides, for the transition or rare-earth metals, on the positions of the d
electrons of the chain and besides, for the transition or rare-earth metals, on the positions of the d
![]() and degenerate d
and degenerate d
![]() levels due to the M atom, which are governed by Pauling's electronegativity
(EN) of atom M. For transition or lanthanide metals, the alternations are "even" if
levels due to the M atom, which are governed by Pauling's electronegativity
(EN) of atom M. For transition or lanthanide metals, the alternations are "even" if
![]() (deficient d electron-elements: columns IIIA to VIIA; empty d
(deficient d electron-elements: columns IIIA to VIIA; empty d
![]() and
and
![]() levels) or "odd" in the reverse case (rich d electron elements: column VIIIA bonding d
levels) or "odd" in the reverse case (rich d electron elements: column VIIIA bonding d
![]() and
and
![]() levels). For normal elements, the limit of
EN seems to be the
EN of C (2.5) and the alternations are "even" if
levels). For normal elements, the limit of
EN seems to be the
EN of C (2.5) and the alternations are "even" if
![]() or "odd" in the other case.
or "odd" in the other case.
Résumé
Les agrégats
![]() obtenus à partir de carbures par diverses méthodes expérimentales (SIMS, SSMS, vaporisation laser, effusion de Knudsen à
haute température, etc.) présentent des alternances dans leurs intensités d'émission I(
obtenus à partir de carbures par diverses méthodes expérimentales (SIMS, SSMS, vaporisation laser, effusion de Knudsen à
haute température, etc.) présentent des alternances dans leurs intensités d'émission I(
![]() ) avec maximums pour
n impair si M = H, F, CI ou Fe, Ni, Rh, Ir, Pt ou au contraire pour
n pair si M = B, Si, Ba, Ge ou Sc, Ti, V, Cr, Y, Zr, La, Ce, W, Th, U ou même n'existent que pour
n pair (Nd, Dy, Ho, Er). D'autre part, seuls sont connus CO,
) avec maximums pour
n impair si M = H, F, CI ou Fe, Ni, Rh, Ir, Pt ou au contraire pour
n pair si M = B, Si, Ba, Ge ou Sc, Ti, V, Cr, Y, Zr, La, Ce, W, Th, U ou même n'existent que pour
n pair (Nd, Dy, Ho, Er). D'autre part, seuls sont connus CO,
![]() O, CN et
O, CN et
![]() N pour l'oxygène et l'azote. Ces phénomènes sont interprétés tout d'abord à l'aide de la règle bien connue de correspondance
qui relie de fortes (resp. faibles) intensités ou fréquences d'émissions d'ions
N pour l'oxygène et l'azote. Ces phénomènes sont interprétés tout d'abord à l'aide de la règle bien connue de correspondance
qui relie de fortes (resp. faibles) intensités ou fréquences d'émissions d'ions
![]() à de fortes (resp. faibles) stabilités des amas correspondants. En second lieu, ces résultats s'expliquent dans le cadre
du modèle de Pitzer et Clementi (hybridation sp en théorie de Hückel) corroboré par des calculs CNDO: on suppose que les amas
à de fortes (resp. faibles) stabilités des amas correspondants. En second lieu, ces résultats s'expliquent dans le cadre
du modèle de Pitzer et Clementi (hybridation sp en théorie de Hückel) corroboré par des calculs CNDO: on suppose que les amas
![]() sont des chaînes linéaires
sont des chaînes linéaires
![]() portant un atome d'impureté M en bout de chaîne. Dans ces conditions, les alternances de stabilités relatives des
portant un atome d'impureté M en bout de chaîne. Dans ces conditions, les alternances de stabilités relatives des
![]() proviennent de ce que l'orbitale moléculaire la plus élevée (" HOMO ") se trouve dans une bande niveaux
proviennent de ce que l'orbitale moléculaire la plus élevée (" HOMO ") se trouve dans une bande niveaux
![]() doublement dégénérés et qu'à une orbitale
doublement dégénérés et qu'à une orbitale
![]() complète (4 électrons) correspond une plus forte stabilité de l'amas que si l'orbitale est incomplète. Or le nombre d'électrons
complète (4 électrons) correspond une plus forte stabilité de l'amas que si l'orbitale est incomplète. Or le nombre d'électrons
![]() d'une chaîne
d'une chaîne
![]() est gouverné par le nombre de niveaux
est gouverné par le nombre de niveaux
![]() liants et en outre pour les éléments de transition ou de terres rares, par la position du niveau d
liants et en outre pour les éléments de transition ou de terres rares, par la position du niveau d
![]() et celle du niveau
et celle du niveau
![]() dégénérés dus à la présence de l'atome M. Dans le cas des éléments normaux, si M est plus électronégatif que C (
EN = 2,5), l'orbitale
dégénérés dus à la présence de l'atome M. Dans le cas des éléments normaux, si M est plus électronégatif que C (
EN = 2,5), l'orbitale
![]() sera liante (2 électrons) alors qu'elle sera antiliante (vide) dans le cas contraire, et entraînera donc une différence de
2 électrons
sera liante (2 électrons) alors qu'elle sera antiliante (vide) dans le cas contraire, et entraînera donc une différence de
2 électrons
![]() ou
ou
![]() , donc un changement de sens des alternances. Le cas spécial de H peut aussi s'expliquer dans ce cadre. Les éléments de transition
pour leur part, se scindent en 2 groupes suivant que leur électronégativité
EN est supérieure à 1,7 (éléments ayant beaucoup d'électrons d : colonne VIIIA ; niveaux
, donc un changement de sens des alternances. Le cas spécial de H peut aussi s'expliquer dans ce cadre. Les éléments de transition
pour leur part, se scindent en 2 groupes suivant que leur électronégativité
EN est supérieure à 1,7 (éléments ayant beaucoup d'électrons d : colonne VIIIA ; niveaux
![]() et d
et d
![]() liants) ou non (peu d'électrons d : colonnes IIIA et terres rares à VIIA ; niveaux
liants) ou non (peu d'électrons d : colonnes IIIA et terres rares à VIIA ; niveaux
![]() et d
et d
![]() vides). Nous donnons deux tableaux récapitulant la structure comparée des niveaux des agrégats
vides). Nous donnons deux tableaux récapitulant la structure comparée des niveaux des agrégats
![]() pour les éléments normaux ou de transition. Ce type de structure peut seul expliquer l'origine des alternances des amas
pour les éléments normaux ou de transition. Ce type de structure peut seul expliquer l'origine des alternances des amas
![]() et permet même de prévoir pour des carbures de transition ou de terres rares non encore étudiés, si les alternances seront
" paires "
et permet même de prévoir pour des carbures de transition ou de terres rares non encore étudiés, si les alternances seront
" paires "
![]() ou " impaires "
(EN > 1,7).
ou " impaires "
(EN > 1,7).
© Les Editions de Physique 1991



